

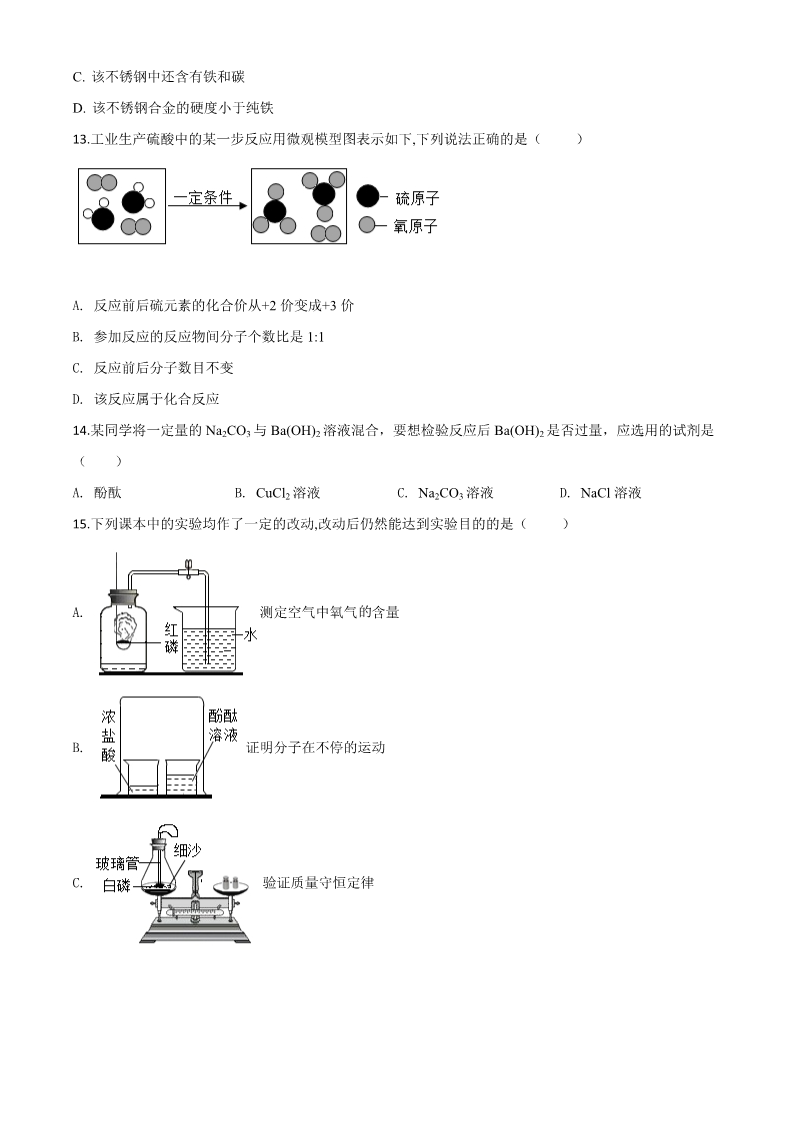


重庆市 2020 年初中学业水平暨高中招生考试 化学试题(A 卷) (全格共四个大题,满分 70 分,与物理共用 120 分钟) 注意事项: 1.试题的答案书写在答题卡上,不得在试题卷上直接作答。 2.作答前认真阅读答题卡上的注意事项。 3.考试结束,由监考人员将试题和答题卡一并收回。 可能用到的相对原子质量:H-1 C-12 O-16 F-19Na-23 S-32 Fe-56 Ba-137 一、选择题(本大题包括 16 个小题,每小题 2 分,共 32 分)每小题只有一个选项符合题意。 1. 中华文字博大精深,下列成语的本意主要涉及化学变化的是( )A. C. B. D. 春风化雨 叶落知秋 火上浇油 滴水成冰 2. 2020 年 6 月,某高速路上一辆液化着油气槽罐车发生爆炸。爆炸产生的以下物质不属于空气污染物的是 ()A. NO2 B. CO C. 粉尘 D. H2O )3. 能源的开发和利用是世界性问题,下列物质被称为最理想清洁能源的是( A. 氢气 B. 天然气 C. 石油 D. 煤 )4. 空气中含①N2 ②O2 ③稀有气体 ④水蒸气等成分,其中与钢铁生锈有关的是( A. ①③ B. ②④ C. ③④ D. ①④ )5. 烧烤是最古老的饮食方法之一,人们喜爱的下列菜品中富含维生素的是( A. 小馒头 B. 鱼 C. 韭菜 D. 五花肉 6. 用溶质质量分数为 36%的浓盐酸配制一定浓度的稀盐酸时,不会用到的仪器是( )A. B. C. D. 7. 化学让我们鉴赏了溶液的颜色美,下列物质加入水中能形成有色溶液的是( )A. B. C. D. 氯化钠 碳酸钙 高锰酸钾 植物油 8. 化学与生活息息相关,下列做法不科学的是( )A. 甲醛大量用于海鲜的防腐 C. 将易拉罐投入可回收垃圾箱 B. 明矾、活性炭用于净水 D. 青少年常喝牛奶补充钙元素 9. 课本中用加入少 Na2SO4 的水进行电解水实验,从该实验中不能获取的信息是( )A. 纯水的导电能力弱 C. 常温下,水的 pH=7 B. 负极产生气体的速率比正极快 D. 水由氢元素和氧元素组成 10. 硝石是主要含 KNO3 的天然矿物,历史上《本草经集注》中对硝石有记载:“强烧之,紫青烟起…云是真硝石 也”。下列有关 KNO3 的叙述不正确的是( )A. 是一种化合物 B. 可用作复合肥料 C. 可能发生分解反应 D. 其溶解度一定大于 NaCl 的溶解度 11. 世卫组织(WHO)发表声明称,地塞米松(C22H29FO3)可挽救新冠肺炎重症患者生命。下列说法正确的是( )A. 地塞米松属于氧化物 B 地塞米松由 4 种元素组成 C. 地塞米松中氢元素的质量分数最大 D. 地塞米松中碳元素与氧元素的质量比为 22:5 12. “中国高铁,世界第一”,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是: 高温 C+2NiO 2Ni+CO ,下列说法错误的是( )2A. 反应中 NiO 发生还原反应 B. 气体产物中可能有 CO C. 该不锈钢中还含有铁和碳 D. 该不锈钢合金的硬度小于纯铁 13. 工业生产硫酸中的某一步反应用微观模型图表示如下,下列说法正确的是( )A. 反应前后硫元素的化合价从+2 价变成+3 价 B. 参加反应的反应物间分子个数比是 1:1 C. 反应前后分子数目不变 D. 该反应属于化合反应 14. 某同学将一定量的 Na2CO3 与 Ba(OH)2 溶液混合,要想检验反应后 Ba(OH)2 是否过量,应选用的试剂是 ()A. 酚酞 B. CuCl2 溶液 C. Na2CO3 溶液 D. NaCl 溶液 15. 下列课本中的实验均作了一定的改动,改动后仍然能达到实验目的的是( )的测定空气中氧气 含量 A. B. 证明分子在不停的运动 C. 验证质量守恒定律 D. 探究燃烧的条件 16. 甲、乙、丙三种固体物质溶解度曲线如下图所示。下列说法错误的是( )A. t1℃时,甲、乙的溶解度都是 25g B. t1℃时,将三种物质的饱和溶液均升温到 t2℃,能析出晶体的是丙 C. 将甲的饱和溶液从 t1℃升高到 t2℃,溶液中溶质的质量分数变为 28.6% D. t3℃时,将 20g 乙加入到 50g 水中充分搅拌后剩余 5g 乙未溶解 二、填空题(本大题包括 5 个小题。共 21 分)。 17. 用下列物质的序号填空。 ①干冰 ②碳酸氢钠 ③熟石灰 (1)发酵粉中常含有______________; (2)用于人工降雨的是____________; (3)常于改良酸性土壤的是________________。 18. 2019 是门捷列夫发现元素周期表的 150 周年,被确定为“世界化学元素周期表年”,图 1 是元素周期表的 部分内容,图 2 是这三种元素的原子结构示意图。 (1)SeO2 的相对分子质量为__________________。 (2)图 2 中硫原子的结构示意图是_____________。 (3)氧、硫、硒三种元素化学性质相似的原因是_____________________________。 (4)画出 O2-离子的结构示意图是_____________。 19. 火是文明的起源,取火的方法,经历了漫长的演变过程。 (1)古代人使用的“火折子”吹气即可燃,“火折子”的制作材料中有硫磺。硫燃烧的化学反应方程式为 ___________________。 (2)1830 年,法国人发明了摩擦火柴,将白磷、硫、KClO3、MnO2 混合做火柴,摩擦生热使白磷燃烧,, 利用白磷燃烧的热量使 KClO3 分解,然后是硫燃烧。该过程中 KClO3 分解的化学反应方程式为 ________________________________。推测摩擦过程中白磷比硫先燃烧的原因是 ________________________________。 (3)19 世纪中期,瑞典人创造出安全火柴,将红磷涂在火柴盒的摩擦面上,硫、KClO3、MnO2 则藏于火 柴头中。火柴划燃的瞬间,火苗异常旺,对产生此现象的原因推测不合理的是______________(填序号)。 A 火柴头里的硫比火柴梗燃烧更剧烈 B MnO2 分解产生氧气助燃 C KClO3 分解产生氧气助燃 20. 今年新冠病毒肆虐全球,抗疫过程我们用到了多种材料。 (1)医用口罩、隔离服、防护罩中的材料大部分是______(填“天然”或“合成”)材料。 (2)修建火神山、雷神山两座医院时,用到了大量铝合金材料,铝合金密度小、硬度大、耐腐蚀。铝制品 的耐腐蚀 原因是_________________________(用化学反应方程式表示)。铝合金中主要含有铝、铜、镁三 种金属,为验证这三种金属的活动顺序,某同学设计了以下 3 个实验: 实验甲中铝丝会出现的现象是____________________________________。实验甲能得出的结论是_______的 金属活动性更强,另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你 的看法是____________(填序号)。 ACB乙、丙都不能省去 乙、丙都可以省去 ,丙可以省去 乙不能省 D,乙可以省去 丙不能省 21. 今后学习常见物质时会从“价”和“类”两个方面进行学习。下图表示铁元素的常见化合价与含铁物质类别 的关系。 (1)X 的物质类别是_____________。 (2)铁和稀硫酸反应生成的含铁化合物属于上图中的___________(填序号)。 (3)某同学想用物质 a 制取物质 b 设计了以下实验步骤 ①物质 a 与稀盐酸反应的化学反应方程式为____________________________。 ②溶液乙中的溶质一定有____________________________。 ③如果向盛有溶液甲的烧杯中滴加 NaOH 溶液至过量,下列图像能正确表示烧杯中溶液质量变化的是 __________(填序号)。 ABCD三、实验题(本大题包括 2 个小题,共 11 分) 22. 二氧化碳的制取与性质是初中化学实验的重要内容,根据下图回答问题。 ①②③ ④ (1)仪器 a 的名称是___________。 (2)实验室用石灰石与稀盐酸反应制取 CO2,应该选择的发生装置是_________(填序号) 的(3)③中,若 X 为澄清石灰水,则③中可以观察到 现象是_________________________。若 X 是水,④中能 观察到紫色石蕊试纸变红,若④中紫色石蕊试纸没有变红,则 X 可能是_______(填序号)。 A NaOH 溶液 B CaCl2 溶液 C 浓硫酸 D 稀盐酸 23. 学习复分解反应发生条件时,小红同学做了下表中的四个实验。 试管编号 ①②③④试管内试剂 NaOH 溶液 MgCl2 溶液 Na2CO3 溶液 Ba(NO3)2 溶液 加入硫酸后的现象 无明显现象 无明显现象 产生气泡 白色沉淀生成 (1)根据以上实验,可以判断试管③④中发生了复分解反应。试管③中反应的化学方程式为 _________________________________。 (2)小明同学向盛有 NaOH 溶液的试管中先加了一种试剂,再加稀硫酸,从而能说明试管①中也发生了反 应,这种试剂是___________。 (3)为了验证试管②中是否发生复分解反应,小明同学进行了如下探究。 [提出猜想]猜想 1:试管②中没有发生复分解反应,溶液中有 MgCl2,即 Mg2+和 Cl-同时存在溶液中。 猜想 2:试管②中发生了复分解反应,溶液中无 MgCl2。 2- 老师提示 SO4 会对 Cl-的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了以下实验方案。 [设计方案] 沉淀 A 的化学式是___________。 老师评价该方案时指出:设计思路正确,但试剂选择有误,你认为应该将所选的试剂_______改成 ____________。 小明按照修改后的方案进行了实验,最后得出的结论是猜想 1 正确,则步骤Ⅱ、步骤Ⅲ中必然会观察到的 现象是____________________。 [实验反思]小明反思进行步骤Ⅲ时,加 NaOH 溶液采用了滴加的方式,但没有立即观察到任何现象,你认 为其中的原因是_______________________。 四、计算题(本大题包括 1 个小题,共 6 分) 24. 过氧化氢溶液俗称双氧水,是一种常见消毒剂。实验员用以下方法制取了少量过氧化氢溶液,在低温下,向 56.4g 某浓度的稀硫酸中逐渐加入一定量的过氧化钡(BaO2),发生的化学反应为 BaO2+H2SO4=BaSO4↓+H2O2, 当恰好完全反应时生成 23.3g 沉淀。计算: (1)加入 BaO2 的质量。 (2)反应后所得溶液中溶质质量分数。 (3)医用双氧水常为溶质质量分数为 3%的过氧化氢溶液,如果将(2)中所得溶液稀释到医用双氧水浓度,计 算需加入水的质量(结果精确到 0.1g)。 本试卷的题干 0635
声明:如果本站提供的资源有问题或者不能下载,请点击页面底部的"联系我们";
本站提供的资源大部分来自网络收集整理,如果侵犯了您的版权,请联系我们删除。





