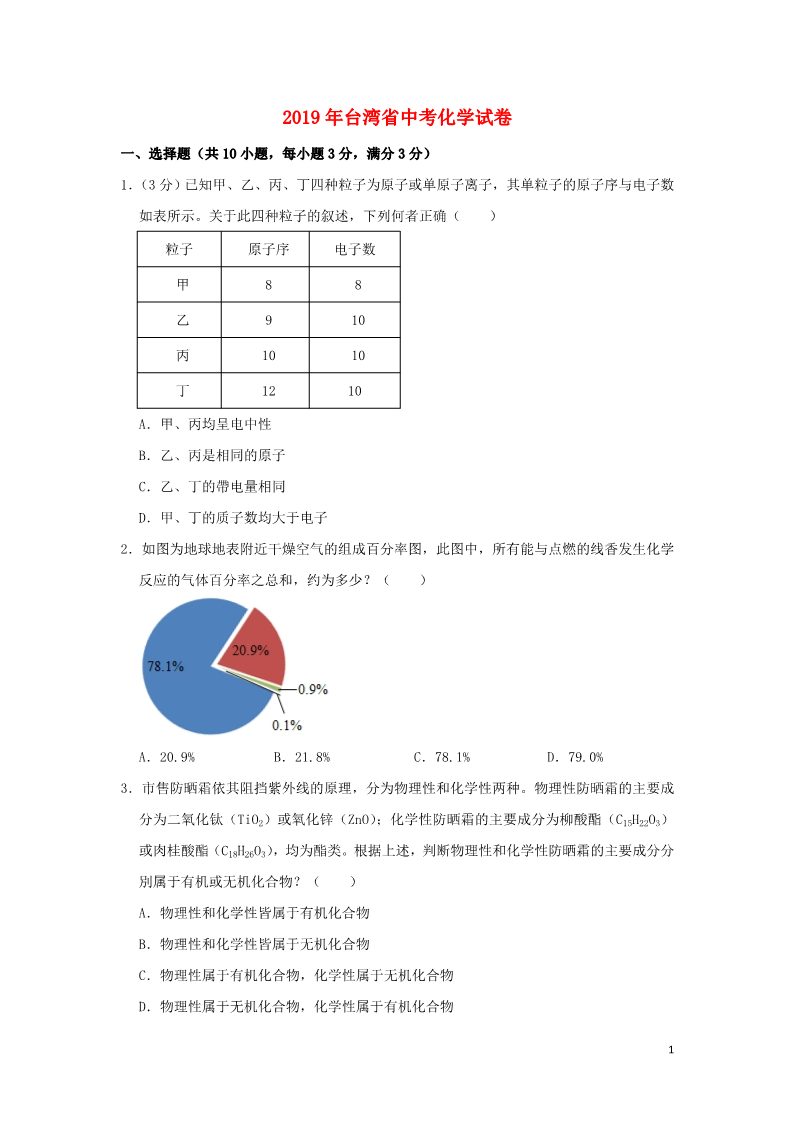


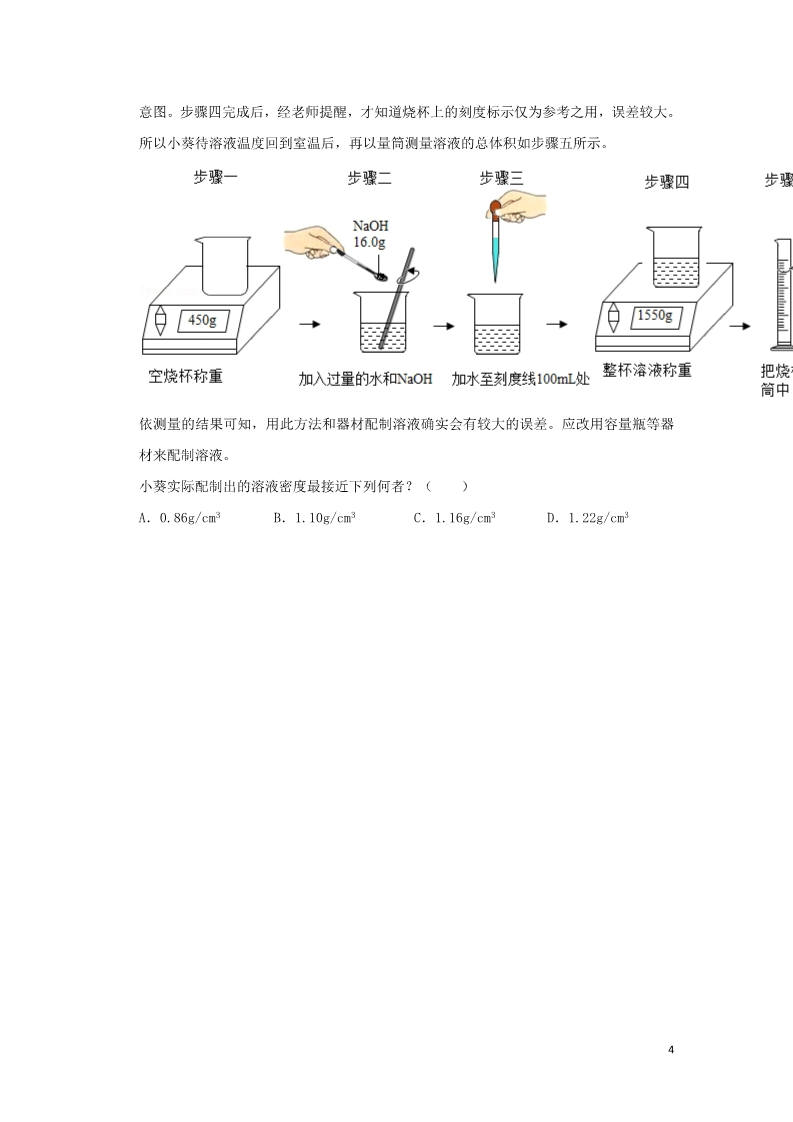

2019年台湾省中考化学试卷 一、选择题(共 10小题,每小题 3分,满分 3分) 1.(3分)已知甲、乙、丙、丁四种粒子为原子或单原子离子,其单粒子的原子序与电子数 如表所示。关于此四种粒子的叙述,下列何者正确( ) 粒子 甲原子序 电子数 89810 10 10 乙丙10 12 丁A.甲、丙均呈电中性 B.乙、丙是相同的原子 C.乙、丁的帶电量相同 D.甲、丁的质子数均大于电子 2.如图为地球地表附近干燥空气的组成百分率图,此图中,所有能与点燃的线香发生化学 反应的气体百分率之总和,约为多少?( ) A.20.9% B.21.8% C.78.1% D.79.0% 3.市售防晒霜依其阻挡紫外线的原理,分为物理性和化学性两种。物理性防晒霜的主要成 分为二氧化钛(TiO2)或氧化锌(ZnO);化学性防晒霜的主要成分为柳酸酯(C15H22O3) 或肉桂酸酯(C18H26O3),均为酯类。根据上述,判断物理性和化学性防晒霜的主要成分分 別属于有机或无机化合物?( ) A.物理性和化学性皆属于有机化合物 B.物理性和化学性皆属于无机化合物 C.物理性属于有机化合物,化学性属于无机化合物 D.物理性属于无机化合物,化学性属于有机化合物 14.「这辆机车所载运的物质为纯氧,危险性较低…」上述为某机车发生交通事故时,消防人 员所说的一段话。根据上述内容,机车所载运的化学物质最可能会在图元素周期表中的 甲、乙、丙和丁哪一个区域内?( ) A.甲 B.乙 C.丙 D.丁 5.部分市售的防蚊产品以品以「敌避」为主要成分,「敌避」分子式为 X12H17NO,熔点为﹣ 45℃,沸点为 290℃,是一种具有驱蚊功效的物质。在常温常压下,「敌避」应属于下列 何种物质?( ) A.液体聚合物 B.液体化合物 C.固体聚合物 D.固体化合物 6.液态 N2O4与 N2H4是火箭常使用的燃料。这二种物质混合并于适当条件下反应,可产生 N2、H2O及大量热能,而得以推动火箭顺利升空。上述反应中,关于 N2O4的叙述,下列何 者正确?( ) A.因进行氧化反应,所以为氧化剂 B.因进行氧化反应,所以为还原剂 C.因进行还原反应,所以为氧化剂 D.因进行还原反应,所以为还原剂 7.取相同莫耳数的丙酮(CH3COCH3)、丙烷(C3H3)分別与氧气反应,未平衡系数的反应式 如下: CH3COCH3+O2→CO2+H2O C3H8+O2→CO2+H2O 若丙酮和丙烷皆完全燃烧,则上述两种反应的氧气消耗量和水生成量之间关系,应为下 列何者?( ) A.氧气消耗量:丙酮<丙烷;水生成量:丙酮<丙烷 B.氧气消耗量:丙酮<丙烷;水生成量:丙酮>丙烷 2C.氧气消耗量:丙酮>丙烷:水生成量:丙酮<丙烷 D.氧气消耗量:丙酮>丙烷;水生成量:丙酮>丙烷 8.杂志上的一篇报导如下:「(一)海水因二氧化碳等非金属氧化物的增加而酸化,严重影 响珊瑚和其他分泌碳酸钙的海洋生物生存。(二)因海水氢离子的浓度増加,这些海洋生 物的碳酸钙外壳可能会遭到分解。」关于此报导画底线处内容的判断与解释,下列何者正 确?( ) A.第(一)句合理,因为这些氧化物溶于海水中会使海水 pH值增加 B.第(一)句不合理,因为这些氧化物溶于海水中会使海水 pH值下降 C.第(二)句合理,因为这些海洋生物的碳酸钙外壳会与氢离子反应 D.第(二)句不合理,因为这些海洋生物的碳酸钙外壳不会与氢离子反应 9.请阅读下列叙述后。回答问题。 小葵查询相关资料后,知道要配制某种浓度的 NaOH水溶液 100mL,需加入 NaOH 16.0g。 如图的步骤一至步骤四为她在室温下进行此浓度溶液配制,以及溶液密度测量的步骤示 意图。步骤四完成后,经老师提醒,才知道烧杯上的刻度标示仅为参考之用,误差较大。 所以小葵待溶液温度回到室温后,再以量筒测量溶液的总体积如步骤五所示。 依测量的结果可知,用此方法和器材配制溶液确实会有较大的误差。应改用容量瓶等器 材来配制溶液。 小葵原本想配制的溶液体积莫耳浓度,以及实际配制出的浓度依序为何?(H、O和 Na的 原子量分别为 1、16和 23) A.0.4M、小于 0.4M B.0.4M、大于 0.4M D.4.0M、大于 4.0M C.4.0M、小于 4.0M 10.请阅读下列叙述后。回答问题 小葵查询相关资料后,知道要配制某种浓度的 NaOH水溶液 100mL,需加入 NaOH 16.0g。 如图的步骤一至步骤四为她在室温下进行此浓度溶液配制,以及溶液密度测量的步骤示 3意图。步骤四完成后,经老师提醒,才知道烧杯上的刻度标示仅为参考之用,误差较大。 所以小葵待溶液温度回到室温后,再以量筒测量溶液的总体积如步骤五所示。 依测量的结果可知,用此方法和器材配制溶液确实会有较大的误差。应改用容量瓶等器 材来配制溶液。 小葵实际配制出的溶液密度最接近下列何者?( ) A.0.86g/cm3 B.1.10g/cm3 C.1.16g/cm3 D.1.22g/cm3 42019年台湾省中考化学试卷 参考答案与试题解析 一、选择题(共 10小题,每小题 3分,满分 3分) 1.(3分)已知甲、乙、丙、丁四种粒子为原子或单原子离子,其单粒子的原子序与电子数 如表所示。关于此四种粒子的叙述,下列何者正确( ) 粒子 甲原子序 电子数 89810 10 10 乙丙10 12 丁A.甲、丙均呈电中性 B.乙、丙是相同的原子 C.乙、丁的帶电量相同 D.甲、丁的质子数均大于电子 【解答】解:A、甲和丙的原子序数等于核外电子数,则原子均呈电中性,故正确; B、乙和丙的原子序数不同,属于不同原子,故错误; C、乙中原子序数=9<电子数=10,带一个单位的负电荷,丁中原子序数 12>电子数= 10,带两个单位的负电荷,可知乙、丁带电量不同,故错误; D、甲中质子数=电子数,丁中质子数<电子数,故错误; 故选:A。 【点评】原子由原子核和核外电子构成,其中原子核由质子和中子构成的,质子带正电 荷,中子不带电,原子的质量主要集中在原子核上。 2.如图为地球地表附近干燥空气的组成百分率图,此图中,所有能与点燃的线香发生化学 反应的气体百分率之总和,约为多少?( ) 5A.20.9% B.21.8% C.78.1% D.79.0% 【解答】解:由图示可知图中 20.9%表示的是氧气,氧气具有助燃性,所以能与点燃的线 香发生化学反应的气体百分率之总和是 20.9%。 故选:A。 【点评】解答本题关键是熟悉空气的组成。 3.市售防晒霜依其阻挡紫外线的原理,分为物理性和化学性两种。物理性防晒霜的主要成 分为二氧化钛(TiO2)或氧化锌(ZnO);化学性防晒霜的主要成分为柳酸酯(C15H22O3) 或肉桂酸酯(C18H26O3),均为酯类。根据上述,判断物理性和化学性防晒霜的主要成分分 別属于有机或无机化合物?( ) A.物理性和化学性皆属于有机化合物 B.物理性和化学性皆属于无机化合物 C.物理性属于有机化合物,化学性属于无机化合物 D.物理性属于无机化合物,化学性属于有机化合物 【解答】解:二氧化钛(TiO2)或氧化锌(ZnO)中都没有碳元素,属于无机物;柳酸酯 (C15H22O3)和肉桂酸酯(C18H26O3)都含有碳元素,属于有机物。 故选:D。 【点评】解答本题关键是熟悉有机物的判断方法。 4.「这辆机车所载运的物质为纯氧,危险性较低…」上述为某机车发生交通事故时,消防人 员所说的一段话。根据上述内容,机车所载运的化学物质最可能会在图元素周期表中的 甲、乙、丙和丁哪一个区域内?( ) 6A.甲 B.乙 C.丙 D.丁 【解答】解:由题目内容可知,氧元素位于乙区域; 故选:B。 【点评】本题主要考查氧气的性质,不能燃烧,具有助燃性。 5.部分市售的防蚊产品以品以「敌避」为主要成分,「敌避」分子式为 X12H17NO,熔点为﹣ 45℃,沸点为 290℃,是一种具有驱蚊功效的物质。在常温常压下,「敌避」应属于下列 何种物质?( ) A.液体聚合物 B.液体化合物 C.固体聚合物 D.固体化合物 【解答】解:敌避的分子式为 X12H17NO,熔点为﹣45℃,沸点为 290℃,是一种具有驱蚊 功效的物质;在常温常压下,敌避属于液体化合物; 故选:B。 【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物等基本 概念,并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空题中。 6.液态 N2O4与 N2H4是火箭常使用的燃料。这二种物质混合并于适当条件下反应,可产生 N2、H2O及大量热能,而得以推动火箭顺利升空。上述反应中,关于 N2O4的叙述,下列何 者正确?( ) A.因进行氧化反应,所以为氧化剂 B.因进行氧化反应,所以为还原剂 C.因进行还原反应,所以为氧化剂 D.因进行还原反应,所以为还原剂 【解答】解:液态 N2O4与 N2H4反应的化学方程式为: 2N2H4+N2O 2N2↑+4H2O,N2H4 中氮元素的化合价为﹣2价,生成 N2,化合价升高,发生氧化反应,是还原剂;N2O4中氮 元素的化合价为+4价,生成 N2,化合价降低,发生还原反应,是还氧化剂; 7故选:C。 【点评】本题考查了氧化、还原反应,氧化剂、还原剂等知识,知道化合价升高发生氧 化反应,是还原剂;化合价降低发生还原反应,是氧化剂,是解决本题的关键。 7.取相同莫耳数的丙酮(CH3COCH3)、丙烷(C3H3)分別与氧气反应,未平衡系数的反应式 如下: CH3COCH3+O2→CO2+H2O C3H8+O2→CO2+H2O 若丙酮和丙烷皆完全燃烧,则上述两种反应的氧气消耗量和水生成量之间关系,应为下 列何者?( ) A.氧气消耗量:丙酮<丙烷;水生成量:丙酮<丙烷 B.氧气消耗量:丙酮<丙烷;水生成量:丙酮>丙烷 C.氧气消耗量:丙酮>丙烷:水生成量:丙酮<丙烷 D.氧气消耗量:丙酮>丙烷;水生成量:丙酮>丙烷 【解答】解:设 1莫耳丙酮消耗氧气的质量为 x,生成水的质量为 y;1莫耳丙烷消耗氧 气的质量为 m,生成水的质量为 n。 CH3COCH3+3O2→3CO2+3H2O 1莫耳 1莫耳 96 54 xyx=96g y=54g C3H8+5O2→3CO2+4H2O 1莫耳 160 72 1莫耳 mnm=160g n=72g 所以,氧气消耗量:丙酮<丙烷;水生成量:丙酮<丙烷 故选:A。 【点评】本题是一道根据化学方程式的简单计算,利用物质之间的关系进行相应的计算。 88.杂志上的一篇报导如下:「(一)海水因二氧化碳等非金属氧化物的增加而酸化,严重影 响珊瑚和其他分泌碳酸钙的海洋生物生存。(二)因海水氢离子的浓度増加,这些海洋生 物的碳酸钙外壳可能会遭到分解。」关于此报导画底线处内容的判断与解释,下列何者正 确?( ) A.第(一)句合理,因为这些氧化物溶于海水中会使海水 pH值增加 B.第(一)句不合理,因为这些氧化物溶于海水中会使海水 pH值下降 C.第(二)句合理,因为这些海洋生物的碳酸钙外壳会与氢离子反应 D.第(二)句不合理,因为这些海洋生物的碳酸钙外壳不会与氢离子反应 【解答】解:海水中二氧化碳等非金属氧化物的增加,可使海水中酸性增强,从而使海 水酸化,pH增大,第(一)句合理,因为这些氧化物溶于水使海水 pH降低,故 A、B均 错误; 海水中氢离子和碳酸钙可发生反应,可使海洋生物中碳酸钙外壳分解,第(二)句合理, 故 C正确,D错误; 故选:C。 【点评】本题主要考查酸的性质,酸性越强,pH越小。 9.请阅读下列叙述后。回答问题。 小葵查询相关资料后,知道要配制某种浓度的 NaOH水溶液 100mL,需加入 NaOH 16.0g。 如图的步骤一至步骤四为她在室温下进行此浓度溶液配制,以及溶液密度测量的步骤示 意图。步骤四完成后,经老师提醒,才知道烧杯上的刻度标示仅为参考之用,误差较大。 所以小葵待溶液温度回到室温后,再以量筒测量溶液的总体积如步骤五所示。 依测量的结果可知,用此方法和器材配制溶液确实会有较大的误差。应改用容量瓶等器 材来配制溶液。 9小葵原本想配制的溶液体积莫耳浓度,以及实际配制出的浓度依序为何?(H、O和 Na的 原子量分别为 1、16和 23) A.0.4M、小于 0.4M C.4.0M、小于 4.0M B.0.4M、大于 0.4M D.4.0M、大于 4.0M 【解答】解:16.0g氢氧化钠物质的量: =0.4mol, =4mol/L, 小葵原本想配制的溶液体积莫耳浓度: 实际溶液体积是 0.095L, 实际配制出的浓度: =4.2mol/L, 因此小葵原本想配制的溶液体积莫耳浓度,以及实际配制出的浓度依序为 4.0M、大于 4.0M。 故选:D。 【点评】本题主要考查计算方面的问题,计算时要注意规范性和准确性。 10.请阅读下列叙述后。回答问题 小葵查询相关资料后,知道要配制某种浓度的 NaOH水溶液 100mL,需加入 NaOH 16.0g。 如图的步骤一至步骤四为她在室温下进行此浓度溶液配制,以及溶液密度测量的步骤示 意图。步骤四完成后,经老师提醒,才知道烧杯上的刻度标示仅为参考之用,误差较大。 所以小葵待溶液温度回到室温后,再以量筒测量溶液的总体积如步骤五所示。 依测量的结果可知,用此方法和器材配制溶液确实会有较大的误差。应改用容量瓶等器 材来配制溶液。 小葵实际配制出的溶液密度最接近下列何者?( ) A.0.86g/cm3 B.1.10g/cm3 C.1.16g/cm3 D.1.22g/cm3 10 【解答】解:溶液质量:155.0g﹣45.0g=110g, 溶液体积:95mL=95cm3, 小葵实际配制出的溶液密度: =1.16g/cm3, 故选:C。 【点评】本题主要考查计算方面的知识,计算时要注意规范性和准确性。 11
声明:如果本站提供的资源有问题或者不能下载,请点击页面底部的"联系我们";
本站提供的资源大部分来自网络收集整理,如果侵犯了您的版权,请联系我们删除。





