


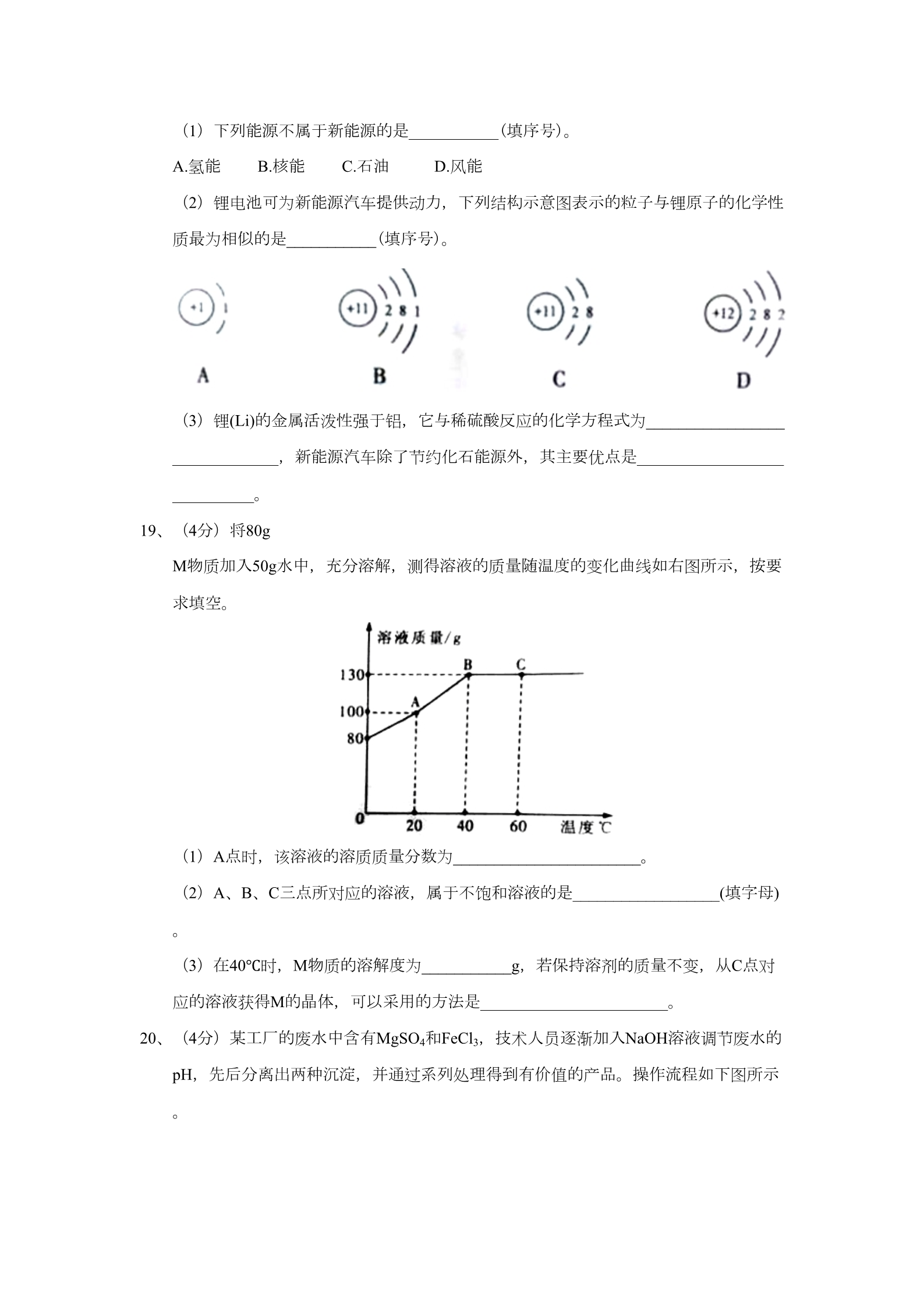

可能用到的相对原子质量:H 1O 16Na 23Mg 24S 32C1 35.5Ca 40 一、选择题(本大题包括16个小题,每小题2分,共32分)每小题只有一个选项符合题意。 1、“绿水青山就是金山银山”。下列物质的大量排放不违背该理念的是 A.氮气 2、端午节吃粽子是传统习俗,在制作粽子的过程中一定发生了化学变化的是 A.水洗糯米 B.刀切肉块 C.粽叶包粽 D.烧火煮粽 3、安全事故无小事。下图是一种危险化学品警示标记,在运输时应张贴该标记的是 B.二氧化硫 C.固体粉尘 D.工业废水 A.食盐 B.鞭炮 C.烧碱 D.酒精 4、我市拥有丰富的页岩气,它与天然气的主要成分相同。下列关于页岩气的说法不正确的 是A.它是混合物 C.它的主要成分是种有机物 5、“关爱生命,拥抱健康”是人类永恒的主题,下列说法不科学的是 A.加铁酱油可预防贫血病 B.用亚硝酸钠代替食盐腌制腊肉 C.甲醛有防腐作用,但不能浸泡食材 D.煮沸是降低硬水硬度的方法之一 B.它是不可再生能源 D.加压使它液化,其分子间的间距不变 6、化学实验操作应严谨规范,下列操作符合要求的是 7、某品牌的小食品贴有如右图所示的标签,从营养均衡的角度分析,该食品还缺少的营养 素是 A.维生素 B.蛋白质 C.油脂 D.糖类 8、水是生命之源,下列关于水的说法不正确的是 A.水是一种化学资源 B.水是一种常用溶剂 C.活性炭在净水过程中起着吸附和消毒作用 D.水在通电的条件下分解得到两种单质 9、王林同学喜欢做化学实验,下图是他给化学药品贴的标签,其中不正确的是 10、碳12是指含6个中子的碳原子。下列对氧16和氧18两种氧原子的说法正确的是 A.质子数相同 B.质量相同 C.电子数不相同 D.16和18表示原子个数 11、研发高性能“中国芯”是我国信息产业的当务之急。“中国芯”的主要材料是高纯度的单 质硅,工业上用SiO2+2C A.生成CO的原因是O2不足 Si+2CO↑来制取粗硅,下列说法正确的是 B.该反应为置换反应 C.硅元素在地壳中的含量比氧元素多 D.该反应体现了C的氧化性 12、民间常用川乌、草乌泡制药酒。川乌、草乌含有少量有毒物质乌头碱(化学式为C34H47 NO11),药酒使用不当会造成中毒。下列关于乌头碱的说法不正确的是 A.乌头碱由四种元素组成 B.乌头碱分子中C、H原子个数比为34:47 C.乌头碱在空气中充分燃烧只生成CO2和H2O D.每个乌头碱分子由93个原子构成 13、实验室常用2KClO3 A. MnO2加快了反应速率 2KCl+3O2↑来制取O2,下列说法错误的是 B.该反应属于分解反应 C.固体减少的质量等于生成O2的质量 D.反应前后氯元素呈现的化合价分别为+3价和-1价 14、食醋里通常含有3-5%的醋酸( CH3COOH),食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列说法不正确 的是 A.产生的气体是二氧化碳 B.加水稀释食醋,溶液pH变小 D.不宜用铝制容器盛装食醋 C.醋酸在水溶液里能解离出H+ 15、纳米铁粉在空气中能自燃并生成一种红色氧化物。对比铁丝在空气中不能燃烧,而在 氧气中能剧烈燃烧的事实,某同学得出的下列结论不正确的是 A.纳米铁粉在空气中自燃的产物不是四氧化三铁 B.相同的反应物在不同条件下生成物可能不同 C.有些物质燃烧时温度不需要达到着火点 D.反应物间的接触面积大小是反应能否发生的因素之一 16、常温下向一定质量的稀盐酸中逐渐加入镁条,充分反应(忽略挥发)。下列图像正确的 是A.①② B.②③ C.①④ D.②④ 二、填空题(本大题包括5个小题,共20分) 17、(4分)江西海昏侯墓考古发掘出大量金器、竹简、玉器和青铜器。某些玉器含有 Al2O3,Al2O3中铝元素显+3价,青铜器上的铜锈可用酸洗,清洗后的溶液中含有铜离 子。 (1)用化学用语表示上面加点的文字为___________和___________。 (2)在下列几种物质中,属于合成材料的是___________(填序号)。 A.竹简 B.棉花 C.塑料 D.青铜 (3)黄金化学性质十分稳定,其外观与铜相似,常用灼烧的方法来鉴别它们,鉴别过 程的化学反应方程式为___________________________________。 18、(4分)新能源汽车的研发和使用是时代发展的需要。 (1)下列能源不属于新能源的是___________(填序号)。 A.氢能 B.核能 C.石油 D.风能 (2)锂电池可为新能源汽车提供动力,下列结构示意图表示的粒子与锂原子的化学性 质最为相似的是___________(填序号)。 (3)锂(Li)的金属活泼性强于铝,它与稀硫酸反应的化学方程式为_________________ _____________,新能源汽车除了节约化石能源外,其主要优点是__________________ __________。 19、(4分)将80g M物质加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如右图所示,按要 求填空。 (1)A点时,该溶液的溶质质量分数为_______________________。 (2)A、B、C三点所对应的溶液,属于不饱和溶液的是__________________(填字母) 。(3)在40℃时,M物质的溶解度为___________g,若保持溶剂的质量不变,从C点对 应的溶液获得M的晶体,可以采用的方法是_______________________。 20、(4分)某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的 pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示 。(1)固体A与某酸反应的化学方程式为______________________________________。 操作②时,当______________即可停止加热。 (2)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为____________ ______。 (3)溶液a除了可能含有NaOH外,还一定含有的溶质是_____________(填化学式)。 21、(4分)2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军 事领域取得重大突破。根据所学知识填空。 (1)建造航母用到了钛合金,构成金属钛的粒子是__________(填“原子”“分子”或“ 离子”),工业制钛有种反应为:TiF4+2H2SO4 的化学式为______________________。 4HF+2X+TiO2,X (2)航母外壳用涂料覆盖,是为了防止钢铁材料与_______________接触而锈蚀。 (3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验( 每步均充分反应),其中能达到目的是________________(填序号)。 A.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉 B.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液 C.ZnCl2溶液中加入足量铜粉后,再加入铁粉 三、实验题(本大题包括2个小题,共11分) 22、(5分)规范使用仪器是实验成功的保障,结合下图所示玻璃仪器,回答问题。 (1)可用作热源的是_____________(填序号),若往仪器E中加入块状固体,则应 先将该仪器________(填“平”“立”或“斜”)放。 (2)若用仪器A和D稀释浓硫酸,则D的作用是________________,若用仪器A和D进 行过滤操作,还必须用到上述的一种仪器是____________(填名称)。 (3)若某气体只能用F装置收集,则该气体的密度比空气小,且___________________ ________。 23、(6分)(1)不同实验对反应速率有不同要求。某同学探究CO2制取实验,按要求答 题。 限选控制反应速率的方法:①反应物的浓度 ②反应物的状态 限选试剂:A.稀盐酸 B.浓盐酸 C.块状石灰石 D.碳酸钠溶液 E.粉末状石灰石 填写下表并回答相关问题。 实验名称 所选用的最佳试剂 ______和D A和C 控制速率的方法 ①灭火器反应原理 CO2的实验室制法 _____________ 写出灭火器反应原理的化学方程式________________________________________。 (2)已知:CO2和SO2既有相似性,又有差异性。 实验一:水槽中滴入紫色石蕊,将收集满两种气体的试管同时倒立于其中,片刻后实 验现象如右图所示,说明相同条件下的溶解性:SO2_____ (填“>”或“<”)CO2,试管内溶液变成______色。 实验二:已知镁条在CO2中剧列燃烧的化学方程式为:2Mg+CO2 2MgO+C,试推 测镁条在SO2中燃烧的现象为:剧烈燃烧,_______________________________。 四、计算题(本大题包括1个小题,共7分) 24、(7分)化学反应在防治环境污染中扮演了重要角色。某工厂废气中的SO2,可用以下 方式处理。方式一:2SO2+O2+2CaO=2CaSO4 方式二:2SO2+O2+4NaOH=2Na2SO4+2H2O 试计算: (已知:CaSO4的价格为700元/吨,相对分子质量为CaSO4 136 Na2SO4 142)。 (1)CaSO4中有两种元素的质量分数呈整数倍关系,这两种元素是硫元素和________ ______。 (2)若用方式一处理9.6tSO2,所得产品价值多少元? (3)若用方式二处理9.61t SO2,刚好用去50t一定浓度的NaOH溶液,求所得溶液的溶质质量分数(最终结果精确 到0.1%)。 一、选择题(本大题包括16个小题,每小题2分,共32分)每小题只有一个选项符合题意。 1-10 ADCDB BACDA11-16 BCDBCC 二、填空题(本大题包括5个小题,共20分) 17、(1)Al2O3 Cu2+ (2)C (3)2Cu+O2 18、(1)C (2)B (3)2Li+H2SO4=Li2SO4+H2↑ 无污染 19、(1)50% 2CuO (2)C (3)160 降温结晶 20、(1)Mg(OH)2+H2SO4=MgSO4+2H2O 还有少量水 (2)H2O (3)NaCl Na2SO4 21、(1)SO3 (2)水、氧气 (3)A 三、实验题(本大题包括2个小题,共11分) 22、(1)C 平(2)搅拌,加速散热 (3)易溶于水 漏斗 23、(1) 实验名称 所选用的最佳试剂 B 和D 控制速率的方法 灭火器反应原理 CO2的实验室制法 ①②A和C Na2CO3+2HCl=2NaCl+CO2↑+H2O (2)> 红产生淡黄色固体 四、计算题(本大题包括1个小题,共7分) (1)氧元素 (2)方式一 解:设9.6tSO2生成CaS04质量为x; 2SO2+O2+2CaO=2CaSO4 128 9.6t 272 x128 272 =9.6 xx=20.4t 产品价值=20.4t×700元/t=14280元 (3)方式二 解:设9.6tSO2生成Na2SO4质量为y; 2SO2+O2+4NaOH=2Na2SO4+2H2O 128 9.6t 284 y128 284 =9.6 yy=21.3t 21.3t ×100%=35.7% 9.6t 50t
声明:如果本站提供的资源有问题或者不能下载,请点击页面底部的"联系我们";
本站提供的资源大部分来自网络收集整理,如果侵犯了您的版权,请联系我们删除。





